- ผู้เขียน Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:41.
- แก้ไขล่าสุด 2025-01-22 17:11.
คุณสามารถแก้หาความเข้มข้นหรือปริมาตรของสารละลายเข้มข้นหรือเจือจางโดยใช้ สมการ : M1V1 = M2V2 โดยที่ M1 คือความเข้มข้นเป็นโมลาริตี (โมล/ลิตร) ของสารละลายเข้มข้น V2 คือปริมาตรของสารละลายเข้มข้น M2 คือความเข้มข้นในโมลาริตีของสารละลายเจือจาง (หลัง
ในทำนองเดียวกัน คุณอาจถามว่าทำไม m1v1 m2v2 ถึงทำงาน
ความเข้มข้นเท่านั้นที่เปลี่ยนแปลง และปริมาตรที่เปลี่ยนแปลง จำนวนโมลของตัวถูกละลายจะคงที่เว้นแต่คุณจะเติมตัวถูกละลายมากขึ้น! ดังนั้นความสัมพันธ์จึงขึ้นอยู่กับข้อเท็จจริงที่ว่าจำนวนโมลของตัวถูกละลายจะคงที่ แต่ความเข้มข้นและปริมาตรของสารละลายทั้งหมดสามารถเปลี่ยนแปลงได้
ต่อมา คำถามคือ คุณใช้สูตร n1v1 n2v2 อย่างไร? N1V1 (HCl)= N2V2 (Na2CO3) หรือ N1× 10 = 0.2 × 25 ∴ N1 = 5 / 10 = 0.5 N Normality × น้ำหนักเทียบเท่า = กำลังเป็นกรัมต่อลิตร 0.5 × 36.5 = 18.25. ความแรงของสารละลาย HCl คือ 18.25 กรัมต่อลิตร
นอกจากนี้ สูตรสำหรับการไทเทรตคืออะไร?
ใช้ สูตรไทเทรต . หากไทแทรนต์และสารวิเคราะห์มีอัตราส่วน 1:1 โมล ค่า สูตร คือโมลาริตี (M) ของกรด x ปริมาตร (V) ของกรด = โมลาริตี (M) ของเบส x ปริมาตร (V) ของเบส (โมลาริตีคือความเข้มข้นของสารละลายที่แสดงเป็นจำนวนโมลของตัวถูกละลายต่อลิตรของสารละลาย)
คุณใช้ m1v1 m2v2 อย่างไร
คุณสามารถแก้หาความเข้มข้นหรือปริมาตรของสารละลายเข้มข้นหรือเจือจาง โดยใช้ สมการ: M1V1 = M2V2 โดยที่ M1 คือความเข้มข้นเป็นโมลาริตี (โมล/ลิตร) ของสารละลายเข้มข้น V2 คือปริมาตรของสารละลายเข้มข้น M2 คือความเข้มข้นในโมลาริตีของสารละลายเจือจาง (หลัง
แนะนำ:
รูปแบบที่ง่ายที่สุดสำหรับ 6 20 คืออะไร?

ลดความซับซ้อนของ 6/20 ให้อยู่ในรูปแบบที่ง่ายที่สุด ออนไลน์ลดความซับซ้อนของเครื่องคิดเลขเศษส่วนเพื่อลด 6/20 เป็นเงื่อนไขต่ำสุดอย่างรวดเร็วและง่ายดาย 6/20 คำตอบแบบง่าย: 6/20 = 3/10
สูตร Sin Cos Tan คืออะไร?
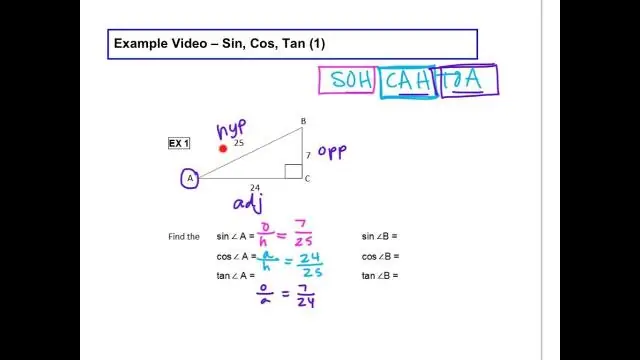
ฟังก์ชันของ sin, cos และ tancan สามารถคำนวณได้ดังนี้: Sine Function:sin(θ) = ตรงข้าม / ด้านตรงข้ามมุมฉาก CosineFunction: cos(θ) = Adjacent / ด้านตรงข้ามมุมฉาก ฟังก์ชันแทนเจนต์: tan(θ) = ตรงข้าม /Adjacent
สูตร c6h12o6 หมายถึงอะไร?

เป็นสูตรทางเคมีของกลูโคส ตัวห้อยตัวเลข (6, 12, 6) ระบุว่ามีอะตอมของคาร์บอน 6 อะตอม ไฮโดรเจน 12 อะตอม และออกซิเจน 6 อะตอมในโมเลกุล C6H12O6 เป็นชื่อทางเคมีของน้ำตาล (ยกเว้นตัวเลขทั้งหมดจะถูกห้อยลงมา)
สูตร mod ใน Excel คืออะไร?
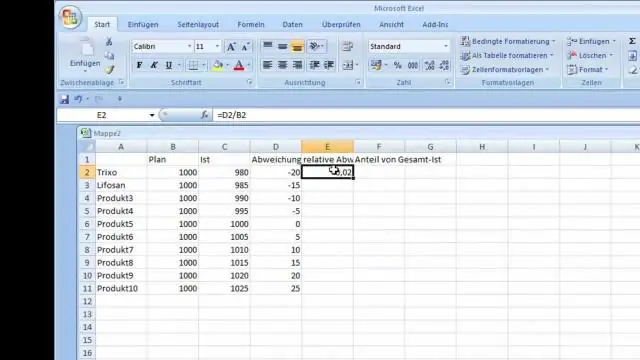
ฟังก์ชัน Microsoft Excel MOD ส่งกลับค่าหลักหลังจากตัวเลขถูกหารด้วยตัวหาร MODfunction เป็นฟังก์ชันในตัวใน Excel ที่จัดประเภทเป็นฟังก์ชันคณิตศาสตร์/ตรีโกณมิติ สามารถใช้เป็นฟังก์ชันแผ่นงาน (WS) ใน Excel
สูตร B 2 4ac คืออะไร?
Discriminant คือนิพจน์ b2 - 4ac ซึ่งกำหนดไว้สำหรับสมการกำลังสอง ax2 + bx + c = 0 โดยอิงจากเครื่องหมายของนิพจน์ คุณสามารถกำหนดจำนวนคำตอบของจำนวนจริงในสมการกำลังสองได้ หากคุณได้จำนวนบวก สมการกำลังสองจะมีคำตอบเฉพาะสองตัว
